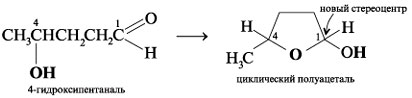
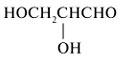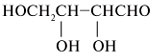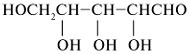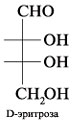Продолжение. Начало см. в № 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 26, Урок 34. Циклические формы моносахаридовИзвестно, что альдегиды и кетоны реагируют со
спиртами, образуя полуацетали и кетали.
Циклические полуацетали образуются особенно
легко. Для этого необходимыми условиями
являются: 1) гидроксил и карбонильная группа
должны быть частями одной молекулы; 2) при их
взаимодействии может образоваться пяти- или
шестичленное кольцо.
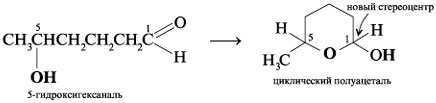
Подобным образом 5-гидроксигексаналь формирует шестичленный циклический полуацеталь, в котором также генерируется новый стереоцентр при С-1:
Гидроксильная и карбонильная группы
содержатся в одной молекуле моносахаридов,
поэтому моносахариды существуют почти
исключительно в форме циклических полуацеталей.
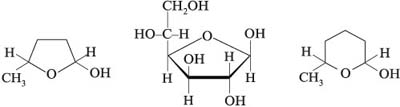
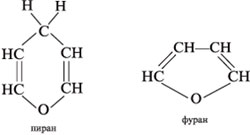
Шестичленные полуацетальные кольца обозначают
словом «пиран», а пятичленные – «фуран».
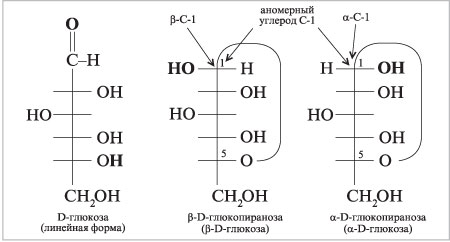
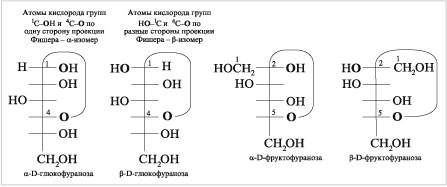
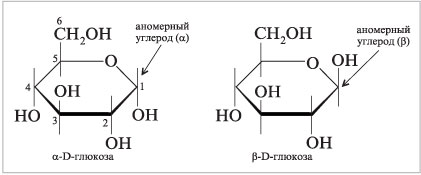
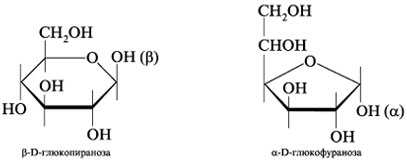
По данным метода ЯМР 13С D-глюкозы
в водном растворе, существуют:
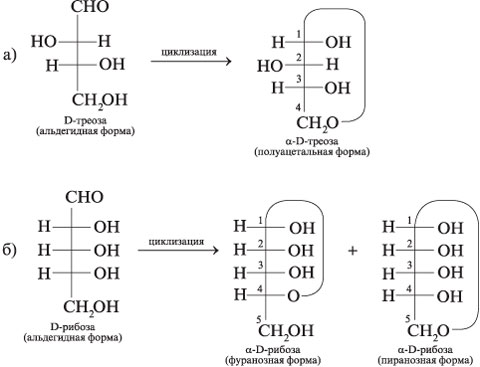
В альдозах замыкание цикла возможно за счет 1-го (альдегидного) углерода и гидроксила при 4-м (или 5-м) атоме С, а в кетозах – за счет 2-го (карбонильного) углерода и гидроксила в 5-м или 6-м положении цепи. Формулы Хеуорса. Альтернативный
способ изображения циклических структур
моносахаридов известен как проекции Хеуорса
и назван так в честь английского химика Уолтера
Хеуорса (нобелевский лауреат, 1937 г.). В формулах
Хеуорса пяти- и шестичленные циклические
полуацетали представляют в виде плоских пяти-
или шестиугольников, расположенных как бы
перпендикулярно плоскости листа бумаги. Группы,
присоединенные к углеродам кольца, располагают
над или под плоскостью кольца и параллельно
плоскости листа бумаги. В формулах Хеуорса
аномерный углерод обычно записывают справа, а
полуацетальный кислород – сзади него. Проекции
Хеуорса
УПРАЖНЕНИЯ. 1. Что означает понятие «циклические формы углеводов»? 2. Приведите структурные и
проекционные формулы Фишера для: а) триозы; б)
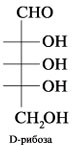
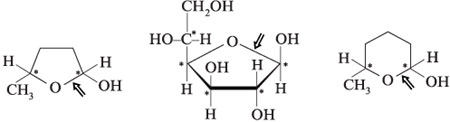
тетрозы; 3. Как по химическим формулам различить L- и D-изомеры (на примере эритрозы)? 4. Укажите ацетальные связи и асимметрические атомы углерода (стереоцентры) в соединениях:
5. Напишите структурные формулы гетероциклов пирана и фурана, указывая каждый атом. 6. Составьте схемы образования
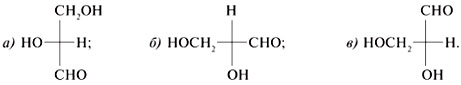
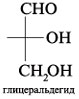
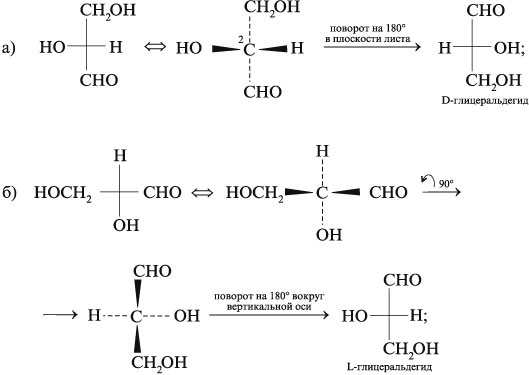
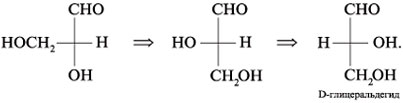
циклических полуацетальных форм из: 7. Преобразуйте графические формулы соединений а)–в) в фишеровские проекции и сделайте отнесение этих проекций к D- или L-глицеральдегиду:
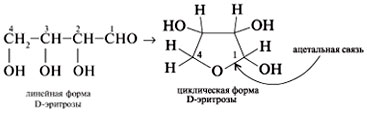
8. Сколько возможно кетотетроз? Для каждой нарисуйте проекции Фишера. 9. Составьте формулы Хеуорса: 1) Ответы на упражнения к теме 2Урок 341. Циклические формы углеводов содержат цикл с кислородом в кольце. Обычно это циклический полуацеталь. В его молекуле нет свободной альдегидной группы, зато имеется ацетальная связь. Например, для эритрозы:
2.
3. Чтобы по химическим
формулам различить D- и L-изомеры эритрозы,
следует представить их в виде проекций Фишера.
Ориентация гидроксила вправо при высшем
стереоцентре С*-3 означает
4. Ацетальные связи отмечены стрелкой (
5.
6.
7.
в) две последовательные перестановки заместителей не изменяют конфигурацию (D или L) при стереоцентре:
8. Возможны две энантиомерные кетотетрозы, для которых проекции Фишера следующие:
9. Формулы Хеуорса:
* Диастереомеры – стереоизомеры, молекулы которых не являются зеркальным отображением друг друга. |