М.А.АХМЕТОВКонспект лекций
|
|
Р РёСЃ. 3.5.
|
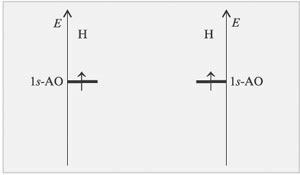
Далее мысленно перекроем две атомные орбитали, образовав две молекулярные, одна из которых (связывающая) обладает меньшей энергией (расположена ниже), а вторая (разрыхляющая) – большей энергией (расположена выше) (рис. 3.6.).
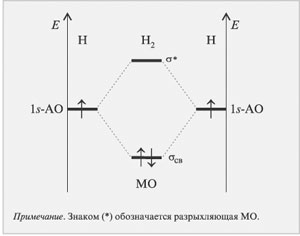 |
Р РёСЃ. 3.6.
|
Видно, что имеется выигрыш в энергии по
сравнению с несвязанными атомами. Свою энергию
понизили оба электрона, что соответствует
единице валентности в методе валентных связей
(связь образуется парой электронов).
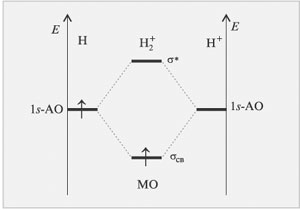
Метод МО ЛКАО позволяет наглядно объяснить
образование ионов ![]() и
и ![]() , что
вызывает трудности в методе валентных связей. На
, что
вызывает трудности в методе валентных связей. На ![]() -связывающую
молекулярную орбиталь катиона
-связывающую
молекулярную орбиталь катиона ![]() переходит один электрон атома H
с выигрышем энергии (рис. 3.7).
переходит один электрон атома H
с выигрышем энергии (рис. 3.7).
|
Р РёСЃ. 3.7.
|
В анионе ![]() на двух молекулярных орбиталях
необходимо разместить уже три электрона
(СЂРёСЃ. 3.8).
на двух молекулярных орбиталях
необходимо разместить уже три электрона
(СЂРёСЃ. 3.8).
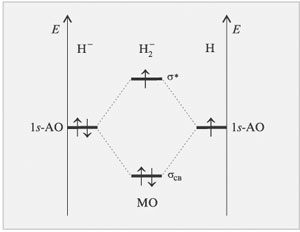 |
Р РёСЃ. 3.8.
|
Если два электрона, опустившись на
связывающую орбиталь, дают выигрыш в энергии, то
третьему электрону приходится повысить свою
энергию. Однако энергия, выигранная двумя
электронами, больше, чем проигранная одним. Такая
частица может существовать.
Рзвестно, что щелочные металлы РІ газообразном
состоянии существуют в виде двухатомных молекул.
Попробуем убедиться в возможности существования
двухатомной молекулы Li2, используя метод МО
ЛКАО. Рсходный атом лития содержит электроны РЅР°
двух энергетических уровнях – первом и втором (1s
Рё 2s) (СЂРёСЃ. 3.9).
|
Р РёСЃ. 3.9.
|
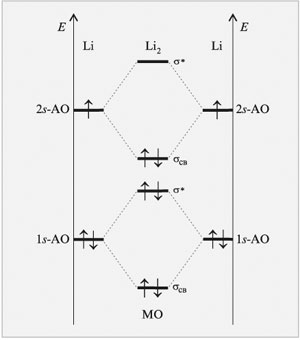
Перекрывание одинаковых 1s-орбиталей
атомов лития даст две молекулярные орбитали
(связывающую и разрыхляющую), которые согласно
принципу минимума энергии будут полностью
заселены четырьмя электронами. Выигрыш в
энергии, получаемый в результате перехода двух
электронов на связывающую молекулярную
орбиталь, не способен компенсировать ее потери
при переходе двух других электронов на
разрыхляющую молекулярную орбиталь. Вот почему
вклад в образование химической связи между
атомами лития вносят лишь электроны внешнего
(валентного) электронного слоя.
Перекрывание валентных 2s-орбиталей атомов
лития приведет также к образованию одной
![]() -связывающей и
одной разрыхляющей молекулярных орбиталей. Два
внешних электрона займут связывающую орбиталь,
обеспечивая общий выигрыш в энергии (кратность
связи равна 1).
-связывающей и
одной разрыхляющей молекулярных орбиталей. Два
внешних электрона займут связывающую орбиталь,
обеспечивая общий выигрыш в энергии (кратность
связи равна 1).
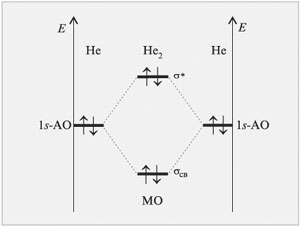
Рспользуя метод РњРћ ЛКАО, рассмотрим возможность
образования молекулы He2 (рис. 3.10).
|
Р РёСЃ. 3.10.
|
В этом случае два электрона займут
связывающую молекулярную орбиталь, а два других
– разрыхляющую. Выигрыша в энергии такое
заселение двух орбиталей электронами не
принесет. Следовательно, молекулы He2 не
существует.
Методом МО ЛКАО легко продемонстрировать
парамагнитные свойства молекулы кислорода. С тем
чтобы не загромождать рисунок, не будем
рассматривать перекрывание 1s-орбиталей
атомов кислорода первого (внутреннего)
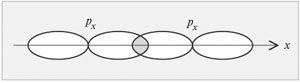
электронного слоя. Учтем, что p-орбитали
второго (внешнего) электронного слоя могут
перекрываться двумя способами. Одна из них
перекроется с аналогичной с образованием ![]() -связи (рис. 3.11).
-СЃРІСЏР·Рё (СЂРёСЃ. 3.11).
|
Р РёСЃ. 3.11.
|
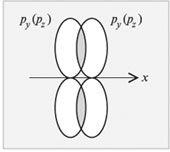
Две других p-АО перекроются по обе
стороны от оси x с образованием двух ![]() -связей (рис. 3.12).
-связей (рис. 3.12).
|
Р РёСЃ. 3.12.
|
Рнергии сконструированных
молекулярных орбиталей могут быть определены по
данным спектров поглощения веществ в
ультрафиолетовой области. Так, среди
молекулярных орбиталей молекулы кислорода,
образовавшихся в результате перекрывания p-АО,
две ![]() -связывающие
вырожденные (с одинаковой энергией) орбитали
обладают меньшей энергией, чем
-связывающие
вырожденные (с одинаковой энергией) орбитали
обладают меньшей энергией, чем ![]() -связывающая, впрочем, как и
-связывающая, впрочем, как и ![]() *-разрыхляющие
орбитали обладают меньшей энергией в сравнении с
*-разрыхляющие
орбитали обладают меньшей энергией в сравнении с
![]() *-разрыхляющей
орбиталью (рис. 3.13).
*-разрыхляющей
орбиталью (рис. 3.13).
|
Р РёСЃ. 3.13.
|
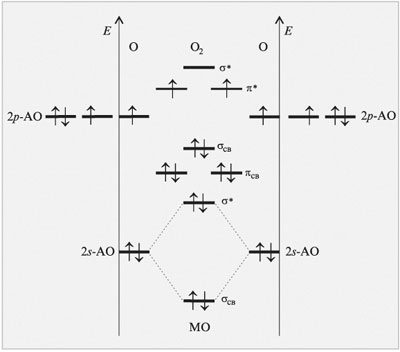
В молекуле O2 два электрона с
параллельными спинами оказались на двух
вырожденных (с одинаковой энергией) ![]() *-разрыхляющих
молекулярных орбиталях. Рменно наличием
неспаренных электронов и обусловлены
парамагнитные свойства молекулы кислорода,
которые станут заметными, если охладить кислород
до жидкого состояния.
*-разрыхляющих
молекулярных орбиталях. Рменно наличием
неспаренных электронов и обусловлены
парамагнитные свойства молекулы кислорода,
которые станут заметными, если охладить кислород
до жидкого состояния.
Среди двухатомных молекул одной из наиболее
прочных является молекула CO. Метод МО ЛКАО легко
позволяет объяснить этот факт (рис. 3.14, см. с.
18).
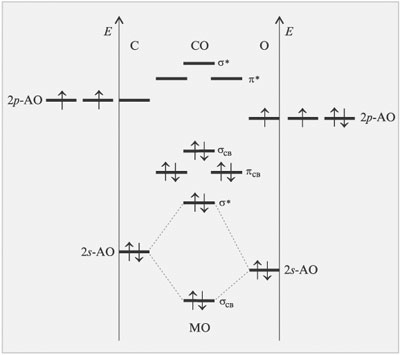 |
Р РёСЃ. 3.14.
|
Результатом перекрывания p-орбиталей
атомов O и C является образование двух
вырожденных
![]() -связывающих и
РѕРґРЅРѕР№
-связывающих и
одной ![]() -связывающей
орбитали. Рти молекулярные орбитали займут шесть
электронов. Следовательно, кратность связи равна
трем.
-связывающей
орбитали. Рти молекулярные орбитали займут шесть
электронов. Следовательно, кратность связи равна
трем.
Метод МО ЛКАО можно использовать не только для
двухатомных молекул, но и для многоатомных.
Разберем в качестве примера в рамках данного
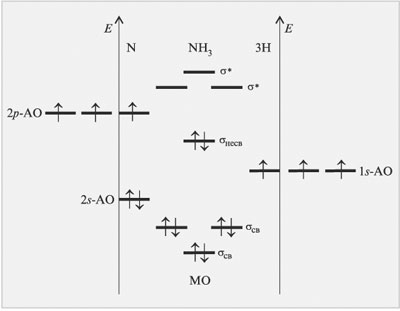
метода строение молекулы аммиака (рис. 3.15).
|
Р РёСЃ. 3.15.
|
Поскольку три атома водорода имеют только три 1s-орбитали, то суммарное число образованных молекулярных орбиталей будет равно шести (три связывающих и три разрыхляющих). Два электрона атома азота окажутся на несвязывающей молекулярной орбитали (неподеленная электронная пара).
3.5. Геометрические формы молекул
Когда говорят о формах молекул, прежде всего имеют в виду взаимное расположение в пространстве ядер атомов. О форме молекулы имеет смысл говорить, когда молекула состоит из трех и более атомов (два ядра всегда находятся на одной прямой). Форма молекул определяется на основе теории отталкивания валентных (внешних) электронных пар. Согласно этой теории молекула всегда будет принимать форму, при которой отталкивание внешних электронных пар минимально (принцип минимума энергии). При этом необходимо иметь в виду следующие утверждения теории отталкивания.
1. Наибольшее отталкивание претерпевают неподеленные электронные пары.
2. Несколько меньше отталкивание между неподеленной парой и парой, участвующей в образовании связи.
3. Наименьшее отталкивание между электронными парами, участвующими в образовании связи. Но и этого бывает недостаточно, чтобы развести ядра атомов, участвующих в образовании химических связей, на максимальный угол.
В качестве примера рассмотрим формы водородных
соединений элементов второго периода: BeH2, BH3,
CH4, C2H4, C2H2, NH3, H2O.
Начнем с определения формы молекулы BeH2.
Рзобразим ее электронную формулу:
H:Be:H,
из которой ясно, что в молекуле отсутствуют
неподеленные электронные пары. Следовательно,
для электронных пар, связывающих атомы, есть
возможность оттолкнуться на максимальное
расстояние, при котором все три атома находятся
на одной прямой, т.е. угол HBeH составляет 180°.
Молекула BH3 состоит из четырех атомов.
Согласно ее электронной формуле в ней
отсутствуют неподеленные пары электронов:
![]()
Молекула приобретет такую форму, при которой расстояние между всеми связями максимально, а угол между ними равен 120°. Все четыре атома окажутся в одной плоскости – молекула плоская:
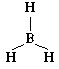
Рлектронная формула молекулы метана выглядит следующим образом:
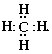
Все атомы данной молекулы не могут оказаться в
одной плоскости. В таком случае угол между
связями равнялся бы 90°. Есть более оптимальное (с
энергетической точки зрения) размещение атомов
– тетраэдрическое. Угол между связями в этом
случае равен 109°28'.
Рлектронная формула этена имеет РІРёРґ:
![]()
Естественно, все углы между химическими
связями принимают максимальное значение – 120°.
Очевидно, что в молекуле ацетилена все атомы
должны находиться на одной прямой:
H:C:::C:H.
Отличие молекулы аммиака NH3 от всех предшествующих состоит в наличии в ней неподеленной пары электронов у атома азота:
![]()
Как уже указывалось, от неподеленной электронной пары более сильно отталкиваются электронные пары, участвующие в образовании связи. Неподеленная пара располагается симметрично относительно атомов водорода в молекуле аммиака:
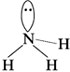
Угол HNH меньше, чем угол HCH в молекуле метана
(вследствие более сильного электронного
отталкивания).
В молекуле воды неподеленных пар уже две:
![]()
Ртим обусловлена уголковая форма молекулы:
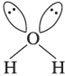
Как следствие более сильного отталкивания
неподеленных электронных пар, угол HOH еще меньше,
чем угол HNH в молекуле аммиака.
Приведенные примеры достаточно наглядно
демонстрируют возможности теории отталкивания
валентных электронных пар. Она позволяет
сравнительно легко предсказывать формы многих
как неорганических, так и органических молекул.
3.6. Упражнения
1. Какие виды связей можно отнести к
химическим?
2. Какие два основных подхода к
рассмотрению химической связи вам известны? В
чем состоит их отличие?
3. Дайте определение валентности и
степени окисления.
4. В чем состоят отличия простой
ковалентной, донорно-акцепторной, дативной,
металлической, ионной связей?
5. Как классифицируют
межмолекулярные связи?
6. Что такое электроотрицательность?
РР· каких данных электроотрицательность
рассчитывается? О чем электроотрицательности
атомов, образующих химическую связь, позволяют
судить? Как изменяется электроотрицательность
атомов элементов при продвижении в
периодической таблице Р”.Р.Менделеева сверху РІРЅРёР·
и слева направо?
7. Какими правилами необходимо
руководствоваться при рассмотрении строения
молекул методом МО ЛКАО?
8. Рспользуя метод валентных связей,
объясните строение водородных соединений
элементов
2-го периода.
9. Рнергия диссоциации РІ СЂСЏРґСѓ молекул
Cl2, Br2, I2 уменьшается
(239 кДж/моль, 192 кДж/моль, 149 кДж/моль
соответственно), однако энергия диссоциации
молекулы F2 (151 кДж/моль) значительно
меньше, чем энергия диссоциации молекулы Cl2,
и выпадает из общей закономерности. Объясните
приведенные факты.
10. Почему при обычных условиях CO2
– газ, а SiO2 – твердое вещество, H2O –
жидкость,
а H2S – газ? Попробуйте объяснить агрегатное
состояние веществ.
11. Рспользуя метод РњРћ ЛКАО, объясните
возникновение и особенности химической связи в
молекулах B2, C2, N2, F2, LiH, CH4.
12. Рспользуя теорию отталкивания
валентных электронных пар, определите формы
молекул кислородных соединений элементов 2-го
периода.