Я иду на урокЖиры и поверхностно-активные
|
Стеарат натрия |
Молекулы ПАВ на пограничной
поверхности располагаются так, что гидрофильные
группы направлены в воду, а гидрофобные
выталкиваются из нее. В результате поверхность
воды покрывается частоколом из молекул ПАВ.
Такая водная поверхность имеет меньшее
поверхностное натяжение, что способствует
быстрому и полному смачиванию загрязненных
поверхностей. Уменьшая поверхность натяжения
воды, мы увеличиваем ее смачивающую способность.
Рассмотрим рисунок, иллюстрирующий процесс
стирки.
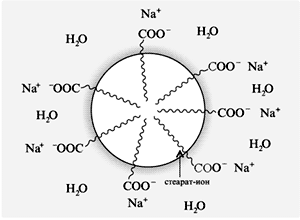 |
Стабилизация стеарат-ионами
|
Покрытая молекулами ПАВ частица
отделяется от поверхности ткани и в виде
эмульсии или суспензии уходит в раствор.
Промышленность выпускает множество различных
СМС-детергентов (моющих средств). Чтобы правильно
пользоваться этими средствами, надо знать, что
разные средства образуют разную среду. Почему?
Ученик. Мыло гидролизуется:
С17Н35СООNa + HOH ![]() С17Н35СООH + NaOH.
С17Н35СООH + NaOH.
Поэтому мылом нельзя стирать шерсть и
натуральный шелк, т. к. при этом белок, из которого
эти волокна состоят, сворачивается и ткань
«садится».
Учитель. Существуют другие СМС, имеющие
нейтральную или слабокислую среду, например:
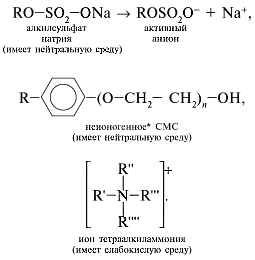
*Неионогенные СМС не диссоциируют в воде на ионы.
Итак, пришло время исследовать моющие вещества, понаблюдать их моющее действие в обычной и жесткой воде. Выполним лабораторный опыт. Описание опыта есть в учебнике. Какие из моющих средств – мыло, стиральный порошок, жидкое СМС – можно использовать дли стирки шерсти и шелка? Почему мыло теряет моющую способность в жесткой воде, а шампунь нет?
Ученик. Стеарат-ион образует с ионами кальция нерастворимую соль:
2С17Н35СОО– + Са2+
= Са(С17Н35СОО)2![]() .
.
СМС образуют растворимые соли кальция, которые
также обладают поверхностно-активными
свойствами.
Учитель. Послушаем сообщение об
экологических последствиях использования ПАВ.
(Ученик рассказывает заранее подготовленное
сообщение.)
Ученик. Многие ПАВ трудно поддаются
биологическому разложению. Поступая со сточными
водами в реки и озера, они загрязняют окружающую
среду. В результате образуются целые горы пены в
канализационных трубах, реках, озерах, куда
попадают промышленные и бытовые стоки.
Использование некоторых ПАВ приводит к гибели
всех живых обитателей в воде. Почему раствор
мыла, попадая в реку или озеро, быстро
разлагается, а некоторые ПАВ нет? Дело в том, что
мыла, полученные из жиров, содержат
неразветвленные углеводородные цепи, которые
разрушаются бактериями. В то же время в состав
некоторых СМС входят алкилсульфаты или
алкил(арил)сульфонаты с углеводородными цепями,
имеющими разветвленное или ароматическое
строение. Такие соединения бактерии
«переварить» не могут. Поэтому при создании
новых ПАВ необходимо учитывать не только их
эффективность, но и способность к биологическому
распаду – уничтожению некоторыми видами
микроорганизмов.
Учитель. Мылом как моющим средством
люди пользуются давно. Уже в XIII в. в России были
мыловарни, а в ряде европейских стран и того
раньше. Домохозяйки во многих странах, а в США
вплоть до 20-х гг. ХХ в. варили жир, смешав его со
щелоком (выпаривали водную вытяжку из золы и
получали щелок), т. е. подвергали жир щелочному
гидролизу. В России в это время мыловарение было
прибыльной мануфактурой. В лавках вовсю
торговали керосином, мылом и другими химическими
товарами.
Чтобы понять, как из жира получить мыло, надо
знать строение жиров. Из чего состоят жиры и
масла, какими свойствами они обладают? Для
выяснения строения существует два метода –
анализ и синтез. Вспомните, как выясняли строение
Н2О:
а) 2Н2О = 2Н2 + О2 (анализ);
б) 2Н2 + О2 = 2Н2О (синтез).
Чтобы выяснить строение жиров, можно поступить
подобным образом. Какой процесс будет являться
синтезом, а какой – анализом?
Ученик. При анализе надо разложить жир
на составные части.
Учитель. Какой процесс будет являться
синтезом?
Ученик. Получение жира из составных
частей.
Учитель проводит демонстрацию гидролиза жира: в
чашку поместить 10 г маргарина и 24 мл 20%-го
раствора NaOH, прилить 7 мл этанола и кипятить 20 мин.
Пока идет реакция, учитель продолжает урок.
Учитель. Откройте учебники и
прочитайте, какие ученые внесли вклад в
установление структуры жиров.
Ученик. М.Шеврель (1817) установил, что
жиры расщепляются и образуют глицерин и
различные карбоновые кислоты. М.Бертло (1854)
синтезировал жир из глицерина и карбоновых
кислот.
По происхождению жиры подразделяют на
растительные и животные.
(Учащиеся приводят примеры растительных и
животных жиров.)
По агрегатному состоянию жиры бывают жидкие –
растительные масла и твердые – животные жиры.
Исключение составляют кокосовое масло (твердое)
и рыбий жир (жидкий).
Учитель. Что происходит с жирами в
организме?
Ученик. Жиры гидролизуются и образуют
карбоновые кислоты и глицерин, а затем из этих
веществ образуются жиры, свойственные данному
живому организму.
Учитель. В состав жидких жиров почти
целиком входят непредельные карбоновые кислоты
– олеиновая С17Н33СООН, линолевая С17Н31СООН,
линоленовая С17Н29СООН, арахидоновая С18Н32СООН.
Эти кислоты незаменимые. Именно они способствуют
окислению твердых жиров в организме, который не
может их синтезировать. Такие кислоты должны
поступать в организм вместе с пищей. В состав
твердых жиров входят остатки предельных
карбоновых кислот: стеариновой С17Н35СООН
и пальмитиновой С15Н31СООН.
Вернемся к нашему опыту и испытаем полученную
смесь на содержание в ней продуктов гидролиза.
Как убедиться в том, что жир прореагировал с
гидроксидом натрия? Какое вещество легко
определить в продуктах гидролиза?
Ученик. Можно определить глицерин с
помощью гидроксида меди(II).
Учитель. К пробе прильем раствор CuSO4,
а затем раствор NaOH. Что наблюдаем?
Ученик. Мы обнаружили глицерин, т. к.
раствор окрасился в фиолетовый цвет.
Учитель. В общем виде процесс гидролиза
можно записать так:
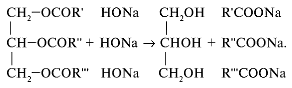
Пользуясь этой схемой, составим уравнение реакции гидролиза жира тристеарина:
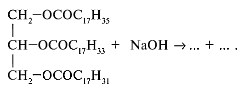
Учащиеся составляют уравнение самостоятельно.
Учитель. Какой это метод исследования
вещества – анализ или синтез?
Ученик. Анализ.
Учитель. Составьте уравнение реакции
синтеза жира.
Учащиеся составляют уравнение в общем виде:
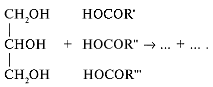
Учитель. Если жидкий жир подвергнуть
гидрированию, т. е. с помощью катализатора
присоединить водород по двойным связям, то
получится твердый жир, называемый саломасом. Его
используют для получения мыла и маргарина. Чтобы
получить маргарин, к саломасу добавляют
сливочное масло, молоко, витамины.
Почему растительные масла имеют короткий срок
хранения по сравнению с твердыми жирами?
Ученик. В составе масел имеются ![]() -связи, по которым
могут происходить реакции окисления.
-связи, по которым
могут происходить реакции окисления.
Учитель. Почему нельзя употреблять
пережаренную пищу?
Ученик. Возможно, что по ![]() -связям происходят какие-то
превращения.
-связям происходят какие-то
превращения.
Учитель. Какие реакции характерны для
непредельных соединений?
Ученик. По ![]() -связям происходят реакции
присоединения и окисления.
-связям происходят реакции
присоединения и окисления.
Учитель. В результате разрыва ![]() -связей при высокой
температуре образуются свободные радикалы,
которые способны вызвать процессы старения в
организме, а также происходит образование
канцерогенных полиароматических соединений.
-связей при высокой
температуре образуются свободные радикалы,
которые способны вызвать процессы старения в
организме, а также происходит образование
канцерогенных полиароматических соединений.
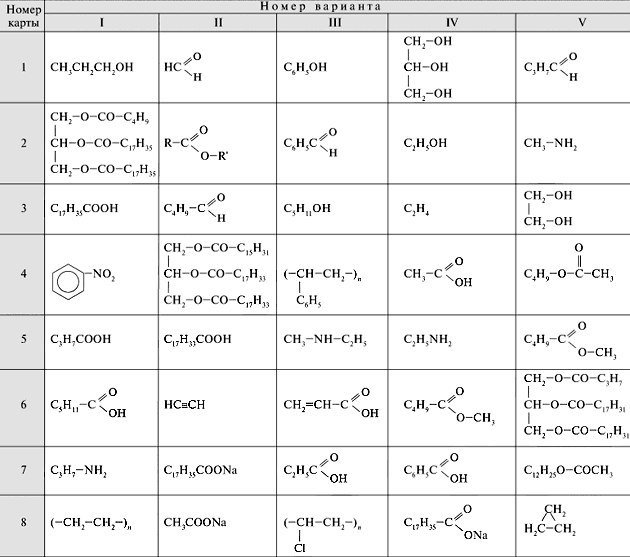
Сейчас по имеющимся у вас картам найдите формулы
жиров. Какие из них твердые, а какие жидкие?
Почему?
Решите задачу (на выбор).
1. Вычислить объем водорода (н. у.), необходимого
для гидрирования 5 моль жира состава II – 4, V – 6
(см. карты с вариантами заданий).
2. Вычислить массу стеарата натрия, полученного
при щелочном гидролизе 3 моль жира состава I – 2.
Домашнее задание. По учебнику
Г.Е.Рудзитиса и Ф.Г.Фельдмана «Химия-10»
(М.: Просвещение, 1991) § 42, упр. 14–16, с. 123.
Литература
Рудзитис Г.Е., Фельдман Ф.Г. Химия-10. М.:
Просвещение, 1991
Артеменко А.И., Тикунова И.В. Органическая
химия. Пробный учебник для 10–11 классов. М.:
Просвещение, 1993;
Перельман Я.И. Знаете ли вы физику? М.:
Просвещение, 1971;
Грин Н., Стаут У., Тейлор Д. Биология. М.: Мир,
1993.
Т.В.ИМЕДЕЕВА,
учитель химии
(г. Тында, Амурская обл.)